
-
大健康企业之十:国网四川电力8.3万员工的“健康管家”是如何炼成的?
2025-09-01
-
胸外科门诊常见问题及回答
2025-09-29
-
大健康企业之十一:加强文体协会建设,带动企业健康发展
2025-10-13
-
大健康企业之九:戈壁滩上的“健康管家”——中国能建葛洲坝三公司大石峡项目医疗保障纪实
2025-08-04
检查发现肺结节,我该怎么办?
作者:北京协和医院胸外科 周梦馨、高雪涵
“肺结节”是如今非常火的一个医学名词。随着全民健康意识的提升,每年常规体检成为大众监测自我健康状况的必要手段,胸部CT是体检中的一个重要环节,很多人在拿到体检报告后,突然发现自己查出了“肺部结节”。那查出了肺结节要怎么办?很多人由于对疾病不了解而产生焦虑,甚至病急乱投医。为此,本文针对“检查发现了肺结节,我该怎么办”这一问题作简要介绍和解答。希望对大家有所帮助。
一、什么是肺结节
肺结节是一个影像学定义,指被肺实质完全包围、界限清楚的小病变(直径≤3cm)。简单来说,就是在影像学检查中发现的肺内的异常病灶。很多肺部疾病都可能表现为肺结节,其中,良性疾病造成的肺结节约占99%1。前面的文章中我们有过详细讲述,因此肺结节并没有想象中可怕。
但是,检查发现了肺结节,请不要慌张,及时到胸外科或呼吸内科就诊,由专业医生进行诊断和治疗,防治恶性病变的遗漏和恶化。
二、诊断
在发现了肺结节后,第一件事应当由专业医生做出初步诊断,具体包括以下两步:
1. 相关科室就诊
能够评估肺结节的科室主要有胸外科和呼吸内科。胸外科以手术作为主要诊断和治疗手段。因此在肺结节方面,胸外科主要评估肺结节需不需手术以及能不能手术。呼吸内科则以非手术方式(主要采用药物治疗)作为主要手段。
图1:胸外科或呼吸内科门诊就诊
每个科室的功能是多样且复杂的,不同科室的诊疗侧重点不同,而且在不同医院,科室的命名也会有差别。因此在就诊之前,可以浏览拟就诊医院的官网,查询不同科室所涉及的疾病范围和主要诊疗手段,选择最适合的科室就诊。
2. 肺结节的评估
肺结节的评估主要涉及三个方面:临床表现、影像学特征及其它辅助检查。
(1)临床表现
临床表现的评估主要通过医生的问诊和简要的查体进行。因此,我们建议患者本人在第一次就诊时到场(至少是进一步治疗前),从而提供最可靠和详尽的第一手资料。而家属和朋友可以进行相应的补充,从而使各项信息更加准确。再者,医生通过与患者的直接沟通,可以解答患者的很多顾虑,让患者本人产生参与感,从而减轻患者对疾病本身以及各种检查和治疗的恐惧心理。
临床表现的评估主要包括以下几点:
患者的症状、体征及针对肺结节的治疗情况:如患者是否有发热、咳嗽、咳痰等不适,是否进行抗感染治疗或中药治疗,以及治疗效果如何等。
患者的基础疾病:如是否患高血压、心脏病、糖尿病及其他恶性肿瘤等。
患者的工作和生活习惯:如是否吸烟、吸烟年限和吸烟量;工作环境是否接触粉尘石棉等有害物质。
患者的家族史:如直系亲属是否患恶性肿瘤等。
(2)影像学特征
影像学特征是评估肺结节过程中最重要的一环。经验丰富的医生,能够根据患者肺结节的影像学特征,给出一个较为准确的诊断。影像学特征的评估主要依靠胸部CT,因此,提供全面且高质量的胸部CT影片非常重要。具体来说,就是将所有的胸部CT影片(从第一次拍片到最近一次拍片)提供给医生,由医生阅片,对结节进行综合评定。
需要评定的特征主要包括以下几点:
结节的大小:结节越大,恶性风险就越高2。对于>2cm的结节,有50%以上的可能是恶性的3。对于>3cm的肺部病变,则被称作“肺肿物”而非“肺结节”,恶性概率更高。
结节的形态:通常形态不规则、边缘粗糙(毛刺、分叶)、牵拉胸膜的结节恶性概率更高4。
结节的密度以及实性成分:根据不同密度及实性成分含量,肺结节可分为实性结节、部分实性结节和纯磨玻璃结节。较小(≤8mm)的实性密度结节通常为良性。和实性结节相比,部分实性结节具有更高的恶性风险。
结节的变化:肺结节增大是结节为恶性肿瘤的独立危险因素。大多数实性的恶性结节体积增大一倍的时间是20-400天5。而磨玻璃结节的体积倍增时间可能更长。需要注意的是,结节增大的评估多数依靠人工测量,这个过程存在误差,通常<1.5mm的变化被认为是误差引起6。
不同的影像学特征对结节性质的判断有一定参考意义,但并不是绝对的。另外,对结节性质的判断主要来源于医生的经验,且会受到很多干扰因素的影响(如CT影片的质量、患者提供信息的准确性等等)。医生给出的诊断是根据资料及病情的经验性判断,而非最终确诊,肺结节唯一的确诊方式是获取结节组织进行病理学检查(如穿刺或手术)。
(3)其它辅助检查
根据不同患者的特点,医生可能会要求患者做一些其他辅助检查,例如肿瘤标记物、PET/CT、肺功能、超声心动图、支气管镜等。
只有各种检查相互辅助和印证,医生才能给出更加准确的诊断并选择最适合患者的治疗方案。
三、治疗
医生经过评估后,一般会对肺结节是良性倾向结节还是恶性倾向结节做出初步判断。不同性质的肺结节会有不同的治疗方案。
1. 良性倾向结节
肺内的良性结节主要包括感染性病变和良性肿瘤。
肺部感染通常需要在呼吸内科进行进一步诊断和针对性的抗感染治疗。如果是陈旧性的肺部感染,可以定期观察。另有一些特殊的肺部感染,如真菌感染或肺结核,抗感染治疗效果有限,这种情况下可以考虑手术治疗。
肺部的良性肿瘤通常都可以选择定期观察。但如果出现了肿瘤进行性增大、肿瘤影响了肺功能或者在定期观察过程中肿瘤出现了恶性征象,则需要根据情况选择手术等诊断和治疗方案。
2. 恶性倾向结节
恶性结节主要包括肺原发恶性肿瘤和肺转移癌。
表现为肺结节的肺原发恶性肿瘤,可根据结节不同的特点、可疑的病理类型及患者的健康状态选择定期观察、手术和其他治疗。
(1)定期观察
对于考虑生长缓慢的恶性倾向结节,即惰性结节,可以暂行观察处理(划重点)。对于初次发现的具有惰性生长特征的结节,推荐3个月后复查胸部CT;如果3个月后结节无明显变化,复查周期可延长至6个月。定期观察的优势在于:患者暂无需经受手术创伤;且如果在随访过程中,结节出现缩小或消失,则结节有很大可能为良性病变。但定期观察可能会成为部分患者的心理负担,严重情况下甚至会影响部分患者正常工作与生活7。这里需要强调的是,对于惰性结节,绝大多数情况下不会在观察期间爆发性生长。因此,在随访过程中,患者无需针对结节做任何治疗措施,调整心态,放松心情,保持健康的生活方式。
(2)手术
经过医生判断,对于存在恶性征象的实性结节,或存在生长征象的部分实性结节和纯磨玻璃结节,需要考虑手术治疗。手术本身兼具诊断和治疗的作用,且对可切除的肺恶性肿瘤治疗效果良好,因此是肺恶性肿瘤治疗中非常重要的一环。
手术方式通常首选经电视胸腔镜辅助(Video-assisted thoracic surgery, VATS)手术或经机器人辅助(Robot-assisted thoracic surgery, RATS)手术,也就是常说的“微创”手术。但是,这里的“微创”仅指手术切口小,手术时间缩短(手术切口和手术时间都是和传统的开胸手术对比),而胸腔内的手术范围并不会缩小。因此,手术风险和术后肺功能的受损都是客观存在的,并不是微创手术就等于“小手术”。
肺恶性肿瘤的标准术式是肿瘤所在的肺叶切除,同时清扫同侧的肺门及纵隔淋巴结。但随着技术的进步以及早期肺癌和癌前病变的检出率增加,亚肺叶切除(即仅切除肺叶的一部分而非整个肺叶,如:肺楔形切除、肺段切除、肺亚段切除等)的应用也越来越广泛。具体选择哪种手术方案,需要由胸外科医生综合评估患者病情后决定。手术方式的决定需要考虑的方面包括但不限于:结节的性质,结节的数量,结节的位置、患者的健康情况等等。
手术之后,整个治疗过程尚未完成。如果术后病理学检查明确了结节为恶性,则需要根据该肿瘤的类型及严重程度(即分期)8进行后续的治疗或随诊。
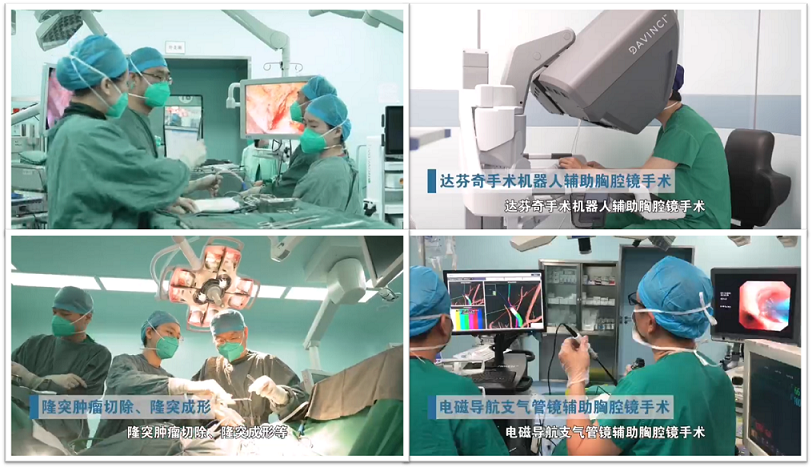
图2:电视辅助胸腔镜手术(VATS)、机器人辅助胸腔镜手术(RATS)、开胸手术及电磁导航支气管镜辅助手术
(3)其他治疗方案
除了手术治疗之外,肺恶性肿瘤还有多种治疗方案,如射频消融术、放疗、化疗、免疫治疗及根据肿瘤的基因检测结果进行靶向治疗。这些治疗方案通常适用于无法进行手术(或拒绝手术)的患者以及作为围手术期的辅助治疗,且这些治疗方案通常需要在明确诊断肺恶性肿瘤后才能进行。
无法手术的情况主要包括两种:
a.考虑晚期病变的结节:如果根据影像学特征及各项辅助检查,医生判定患者失去手术机会(如已存在远处转移、结节侵犯周围大血管或其他脏器),则暂不考虑手术治疗。原因是手术仅增加了患者的创伤而无法达到理想的治疗效果。那么,下一步就是依靠穿刺等方式取得肿瘤组织做病理学检查,根据病理结果决定治疗方案。如果这些治疗方案效果良好,肿瘤缩小,则可由胸外科医生评估手术的难度、风险及获益,决定是否行手术治疗。
b.患者全身状况不允许手术:对于有严重系统性疾病的患者,如严重的冠心病、慢性阻塞性肺疾病等,手术可能造成这些疾病进一步加重,严重时可能危及患者生命。这种情况暂不考虑手术。下一步应就诊于相应科室积极控制系统疾病,通过再次评估决定是否手术。但如果患者的系统性疾病无法得到良好的控制,则同样需要明确病理后,根据病理结果决定下一步治疗方案。
另一类肺恶性结节是肺转移癌,即其他部位的恶性肿瘤发生了肺转移。这类结节的治疗以治疗原发部位肿瘤为主。
四、小结
检查发现了肺结节,首先应就诊于相关科室(通常为胸外科或呼吸内科),由专业医生进行评估;
就诊时,请携带完整且高质量的胸部CT影片和其他辅助检查报告;推荐患者本人就诊;
医生会根据患者临床表现、肺结节的影像学特征及其他辅助检查结果做出初步诊断;
根据结节性质,医生会给出进一步治疗方案,包括定期观察、手术或其他治疗。
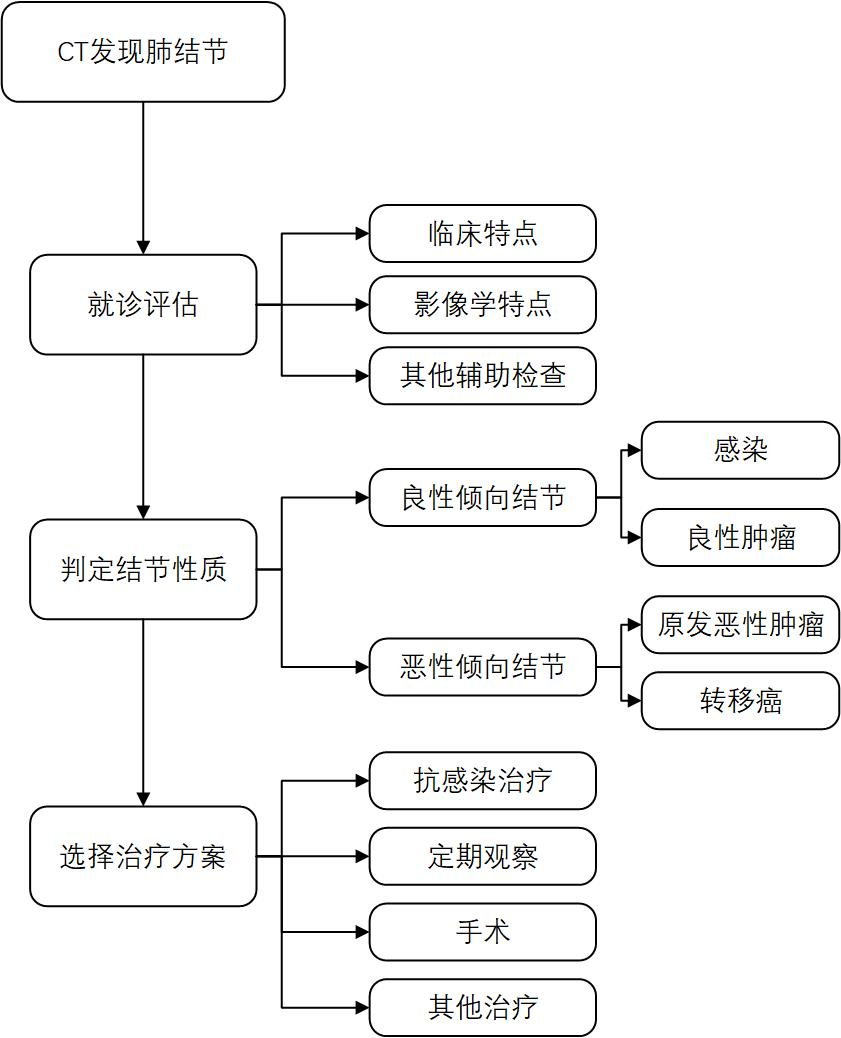
图3:肺结节诊疗流程概述
参考文献
1. McWilliams A, Tammemagi MC, Mayo JR, et al. Probability of cancer in pulmonary nodules detected on first screening CT. N Engl J Med, 2013; 369:910-919.
2. Mehta HJ, Ravenel JG, Shaftman SR, et al. The utility of nodule volume in the context of malignancy prediction for small pulmonary nodules. Chest, 2014; 145:464-472.
3. Gould MK, Fletcher J, Iannettoni MD, et al. Evaluation of patients with pulmonary nodules: when is it lung cancer?: ACCP evidence-based clinical practice guidelines (2nd edition). Chest, 2007; 132:108S-130S.
4. Chu ZG, Li WJ, Fu BJ, Lv FJ. CT Characteristics for Predicting Invasiveness in Pulmonary Pure Ground-Glass Nodules. AJR Am J Roentgenol, 2020; 215:351-358.
5. Thalanayar PM, Altintas N, Weissfeld JL, Fuhrman CR, Wilson DO. Indolent, Potentially Inconsequential Lung Cancers in the Pittsburgh Lung Screening Study. Ann Am Thorac Soc, 2015; 12:1193-1196.
6. Revel MP, Bissery A, Bienvenu M, Aycard L, Lefort C, Frija G. Are two-dimensional CT measurements of small noncalcified pulmonary nodules reliable? Radiology, 2004; 231:453-458.
7. Freiman MR, Clark JA, Slatore CG, et al. Patients' Knowledge, Beliefs, and Distress Associated with Detection and Evaluation of Incidental Pulmonary Nodules for Cancer: Results from a Multicenter Survey. J Thorac Oncol, 2016; 11:700-708.
8. Goldstraw P, Chansky K, Crowley J, et al. The IASLC Lung Cancer Staging Project: Proposals for Revision of the TNM Stage Groupings in the Forthcoming (Eighth) Edition of the TNM Classification for Lung Cancer. J Thorac Oncol, 2016; 11:39-51.




